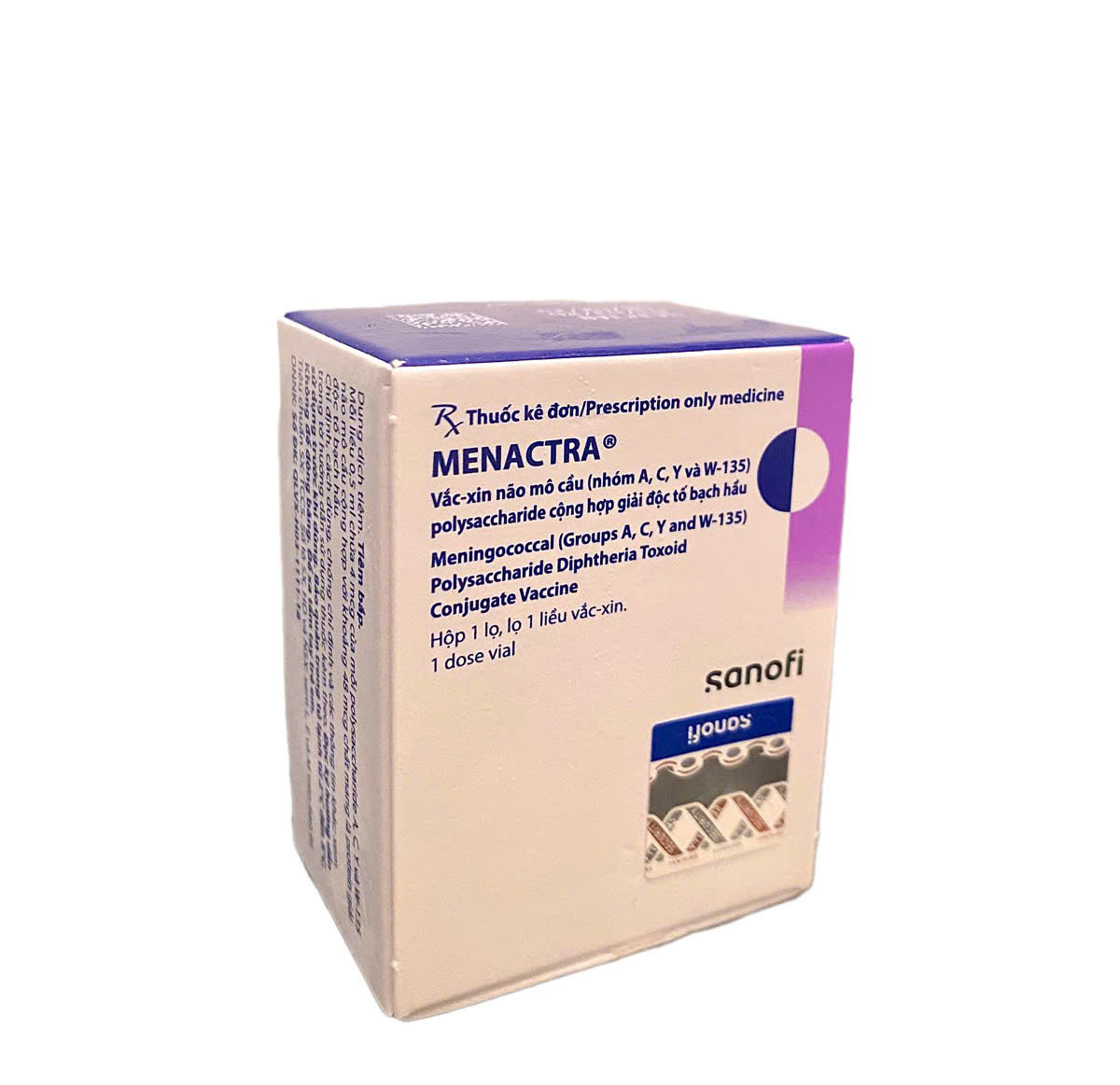
MENACTRA – Vaccine phòng vi khuẩn não mô cầu, nhóm huyết thanh A, C, Y, W-135 (Mỹ)
- Vắc xin phòng vi khuẩn não mô cầu, nhóm huyết thanh A, C, Y, W-135 Menactra (Mỹ)
- Lịch tiêm: (Dưới mô tả)
- Độ tuổi: 9 tháng đến 55 tuổi
- NSX: Sanofi Pasteur (Mỹ)
- Thuốc kê toa: Theo chỉ định của Bác Sĩ
- Giá tiêm tham khảo: 1,300,000 – 1,400,000
-
LH đặt hàng giá sỉ: CÔNG TY CP Y TẾ SÀI GÒNĐiện thoại: 028 3762 6879 – 0905 843 781
Menactra®
Vắc-xin não mô cầu (nhóm A, C, Y và W-135) polysaccharide cộng hợp giải độc tố bạch hầu
Dùng để tiêm. TIÊM BẮP
🖐 Để xa tầm tay trẻ em.
📜 Đọc kỹ hướng dẫn sử dụng trước khi dùng.
⚠ Thông báo ngay cho bác sĩ hoặc dược sĩ những phản ứng có hại gặp phải khi sử dụng vắc-xin.
THÀNH PHẦN
Trong 1 liều 0,5 ml vắc-xin chứa:

Tá dược: Natri clorid, sodium phosphate dibasic anhydrous, sodium phosphate monobasic monohydrate crystal.
DẠNG BÀO CHẾ
- Dung dịch tiêm trong lọ thủy tinh vô khuẩn không có chất bảo quản.
CHỈ ĐỊNH
Menactra được chỉ định để tạo miễn dịch chủ động cơ bản và nhắc lại phòng bệnh xâm lấn do N. meningitidis (Não mô cầu) các nhóm huyết thanh A, C, Y và W-135.
- Được chỉ định để sử dụng ở người từ 9 tháng đến 55 tuổi.
- Menactra không được dùng để điều trị bệnh do não mô cầu.
- Menactra không được sử dụng để điều trị viêm màng não.
- Menactra không được chỉ định để chống lại bệnh bạch hầu.
LIỀU DÙNG VÀ PHÁC ĐỒ SỬ DỤNG
Liều dùng của Menactra là 0,5 ml bằng đường tiêm bắp.
Tiêm chủng cơ bản:
- Trẻ 9 – 23 tháng tuổi: Menactra được tiêm 2 liều cách nhau ít nhất 3 tháng.
- Người ≥ 2 đến 55 tuổi: Tiêm một liều duy nhất.
Tiêm chủng nhắc lại:
- Có thể tiêm một liều nhắc lại cho người từ 15 đến 55 tuổi tiếp tục có nguy cơ mắc bệnh do não mô cầu, nếu liều vắc-xin đầu đã được tiêm ít nhất 4 năm trước đó.
ĐƯỜNG DÙNG VÀ PHƯƠNG PHÁP DÙNG
- Tiêm một liều 0,5 ml Menactra bằng đường tiêm bắp, tốt nhất là tiêm ở mặt trước-ngoài của đùi hoặc vùng cơ delta tùy theo tuổi và khối cơ của đối tượng.
- Không được tiêm tĩnh mạch.
- Tránh tiêm vắc-xin trong vùng hạch đùi vì chưa có nghiên cứu lâm sàng chứng minh tính an toàn và hiệu lực của vắc-xin khi sử dụng ở vị trí này.
CHUẨN BỊ VÀ CÁCH DÙNG
Menactra là sản phẩm dạng lỏng trong suốt đến hơi đục, trong lọ một liều không có chất bảo quản. Trước khi dùng, cần kiểm tra sản phẩm. Vắc-xin cần trông thấy không có tạp chất lạ hoặc biến màu. Không được lắc mạnh lọ vắc-xin hay đun nóng hoặc làm đông đá.
Chuẩn bị:
- Tháo nắp lọ và dùng một bơm tiêm và kim thích hợp, rút 0,5 ml sản phẩm, đảm bảo không có bọt khí trước khi tiêm.
Tiêu hủy:
- Sau khi sử dụng, vắc-xin còn lại và vỏ lọ chứa phải được tiêu hủy một cách an toàn, tốt nhất là bất hoạt bằng nhiệt hoặc hóa chất theo quy trình được chấp thuận ở địa phương.
CHỐNG CHỈ ĐỊNH
- Quá mẫn: Đã biết bị phản ứng quá mẫn toàn thân với bất kỳ thành phần nào của Menactra (như đã ghi trong phần “THÀNH PHẦN” và “CẢNH BÁO VÀ THẬN TRỌNG KHI SỬ DỤNG”) hoặc sau một lần tiêm vắc-xin này hoặc vắc-xin chứa cùng một thành phần trước đây.
- Sốt hay bệnh cấp tính: Trong trường hợp sốt vừa hoặc nặng và/hoặc bệnh cấp tính nên trì hoãn chủng ngừa nếu như không được xem là chống chỉ định.
CẢNH BÁO VÀ THẬN TRỌNG KHI SỬ DỤNG
Không được tiêm vào mạch máu: phải đảm bảo kim tiêm không xuyên vào mạch máu.
Hội chứng Guillain-Barré (GBS)
- Người trước đây đã được chẩn đoán có hội chứng Guillain-Barré (GBS) có thể tăng nguy cơ bị GBS sau khi tiêm Menactra.
- Cân nhắc các yếu tố nguy cơ và lợi ích khi quyết định dùng Menactra.
- Các báo cáo cho thấy nguy cơ GBS sau tiêm Menactra đã được đánh giá thấp hơn nguy cơ bệnh do não mô cầu.
Ngăn ngừa và kiểm soát các phản ứng dị ứng vắc-xin
- Trước khi chỉ định vắc-xin, nhân viên y tế nên xem xét lịch sử tạo miễn dịch của từng cá nhân và kiểm tra khả năng dị ứng.
- Khi các phản ứng quá mẫn xảy ra, phải luôn sẵn sàng ngay lập tức Epinephrine và các chất thích hợp để kiểm soát các phản ứng phản vệ.
Biến đổi khả năng miễn dịch
- Một số đối tượng có thể có đáp ứng miễn dịch kém, bao gồm những đối tượng nhận các phương pháp trị liệu ức chế miễn dịch.
Đặc tính dược động học
Chưa có nghiên cứu dược động học nào được thực hiện.
Quy cách đóng gói
Lọ 1 liều 0,5 ml, hộp 1 lọ.
Điều kiện bảo quản
Bảo quản ở 2°C đến 8°C (35°F đến 46°F) (trong tủ lạnh). KHÔNG ĐƯỢC ĐÔNG BĂNG
Để xa tầm tay trẻ em.
Tuổi thọ
24 tháng ở nhiệt độ 2°C đến 8°C kể từ ngày sản xuất lô vắc-xin.
Hạn dùng
Không được dùng vắc-xin sau ngày hết hạn sử dụng được ghi trên nhãn sau chữ “E”.
Tiêu chuẩn chất lượng
Tiêu chuẩn cơ sở.
Thông tin tư vấn bệnh nhân
Trước khi tiêm vắc-xin Menactra, nhân viên y tế nên cung cấp thông tin cho người định tiêm vắc-xin, cha mẹ, người giám hộ, hoặc người lớn có trách nhiệm về những lợi ích và nguy cơ tiềm tàng đối với bệnh nhân. BÁO CÁO BẤT LỢI VÀ CẢNH BÁO, THẬN TRỌNG KHI SỬ DỤNG. Phải hướng dẫn người định tiêm vắc-xin, cha mẹ hoặc người giám hộ báo cáo Thầy thuốc hoặc những người có chuyên môn y tế, nhân viên y tế về bất kỳ biến cố nào không mong muốn.
Biến cố này cho Sanofi Pasteur qua địa chỉ email: pharmacovigilance.vietnam@sanofi.com và/hoặc hệ thống báo cáo quốc gia gửi đến Trung tâm Quốc gia về thông tin thuốc và theo dõi phản ứng có hại của thuốc theo địa chỉ email: di.pvcenter@gmail.com.
TÊN VÀ ĐỊA CHỈ NHÀ SẢN XUẤT/ĐƠN VỊ ĐƯỢC CẤP GIẤY PHÉP LƯU HÀNH
Sanofi Pasteur
Trụ sở chính: 14 Espace Henry Vallée, 69007 Lyon – Pháp.
Sản xuất bởi: Sanofi Pasteur Inc.
1 Discovery Drive
Swiftwater PA 18370
Hoa Kỳ
Phiên bản: 26/04/2018
Nguồn: Sanofi Pasteur